Si la variante omicron del coronavirus es lo suficientemente diferente de la variante original, es posible que las vacunas existentes no sean tan efectivas como lo han sido.
Si es así, es probable que las empresas necesiten actualizar sus vacunas para combatir mejor el omicron.
Deborah Fuller es una microbióloga que ha estado estudiando vacunas de ARNm y ADN durante más de dos décadas.
Aquí explica por qué es posible que sea necesario actualizar las vacunas y cómo sería ese proceso.
1. ¿Por qué es necesario actualizar las vacunas?
Básicamente, se trata de si un virus ha cambiado lo suficiente como para que los anticuerpos creados por la vacuna original ya no puedan reconocer y defenderse de la nueva variante mutada.
Los coronavirus usan proteínas de pico para unirse a los receptores ACE-2 en la superficie de las células humanas e infectarlas.
Todas las vacunas de ARNm COVID-19 funcionan dando instrucciones en forma de ARNm que dirigen a las células a producir una versión inofensiva de la proteína de pico.
Esta proteína de pico induce al cuerpo humano a producir anticuerpos. Si una persona se expone alguna vez al coronavirus, estos anticuerpos se unen a la proteína del pico del coronavirus y, por lo tanto, interfieren con su capacidad para infectar las células de esa persona.
La variante omicron contiene un nuevo patrón de mutaciones en su proteína de pico .
Estos cambios podrían alterar la capacidad de algunos, pero probablemente no todos, de los anticuerpos inducidos por las vacunas actuales para unirse a la proteína de pico .
Si eso sucede, las vacunas podrían ser menos efectivas para prevenir que las personas se infecten y transmitan la variante omicron.
2. ¿En qué se diferenciaría una nueva vacuna?
Las vacunas de ARNm existentes, como las fabricadas por Moderna o Pfizer, codifican una proteína de pico de la cepa original de coronavirus .
En una vacuna nueva o actualizada, las instrucciones del ARNm codificarían la proteína de pico omicron.
Al intercambiar el código genético de la proteína de pico original por el de esta nueva variante, una nueva vacuna induciría anticuerpos que se unen de manera más efectiva al virus omicron y evitan que infecte las células.
Las personas ya vacunadas o expuestas previamente a COVID-19 probablemente necesitarían solo una única dosis de refuerzo de una nueva vacuna para estar protegidas no solo de la nueva cepa sino también de otras cepas que aún pueden estar en circulación .
Si omicron surge como la cepa dominante sobre delta, los que no estén vacunados solo necesitarían recibir 2-3 dosis de la vacuna actualizada.
Si tanto delta como omicron están en circulación, es probable que las personas reciban una combinación de las vacunas actual y actualizada.
3. ¿Cómo actualizan los científicos una vacuna?
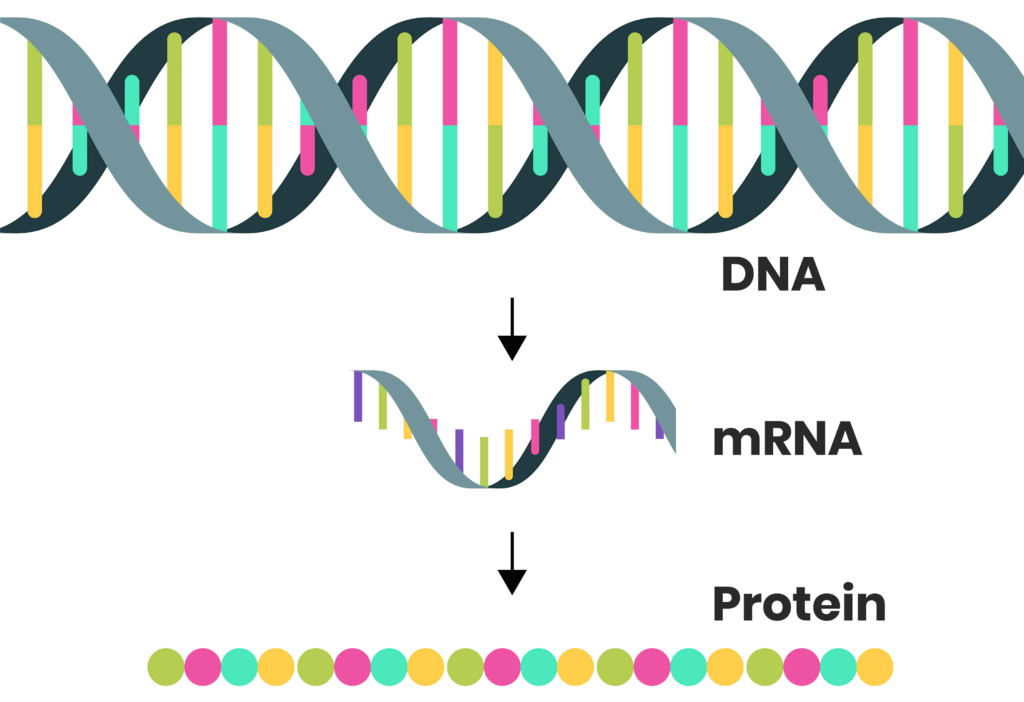
Para hacer una vacuna de ARNm actualizada, necesita dos ingredientes: la secuencia genética de la proteína de pico de una nueva variante de interés y una plantilla de ADN que se usaría para construir el ARNm.
En la mayoría de los organismos, el ADN proporciona las instrucciones para producir ARNm.
Dado que los investigadores ya han publicado el código genético de la proteína de pico omicron , todo lo que queda por hacer es crear una plantilla de ADN para la proteína de pico que se usaría para producir la parte del ARNm de las nuevas vacunas.
Para hacer esto, los investigadores mezclan plantillas de ADN con enzimas sintéticas y cuatro bloques de construcción moleculares que hacen el ARNm – G, A, U y C para abreviar.
Luego, las enzimas construyen una copia de ARNm de la plantilla de ADN, un proceso llamado transcripción. Con este proceso, solo se necesitan unos minutos para producir un lote del ARNm para las vacunas.
Luego, los investigadores colocan las transcripciones de ARNm dentro de nanopartículas grasas que protegen las instrucciones hasta que se entregan de manera segura en las células de su brazo.
4. ¿Cuánto tiempo hasta que esté lista una nueva vacuna?
Solo se necesitan tres días para generar la plantilla de ADN necesaria para hacer una nueva vacuna de ARNm.
Luego, se necesitaría aproximadamente una semana para producir dosis suficientes de la vacuna de ARNm para probar en el laboratorio y otras seis semanas para realizar las pruebas preclínicas en células humanas en tubos de ensayo para asegurarse de que una nueva vacuna funcione como debería.
Entonces, dentro de los 52 días , los científicos podrían tener una vacuna de ARNm actualizada lista para conectarse al proceso de fabricación y comenzar a producir dosis para un ensayo clínico en humanos.
Es probable que ese ensayo requiera al menos otras pocas semanas para un total de alrededor de 100 días para actualizar y probar una nueva vacuna.
Mientras se lleva a cabo ese ensayo, los fabricantes podrían comenzar a cambiar su proceso actual para hacer una nueva vacuna.
Idealmente, una vez que se complete el ensayo clínico, y si la vacuna se autoriza o aprueba, una empresa podría comenzar inmediatamente a distribuir dosis de una nueva vacuna.
5. ¿Una vacuna actualizada necesita ensayos clínicos completos?
Actualmente no está claro cuántos datos clínicos se necesitarían para obtener la aprobación o autorización de la FDA para una vacuna COVID-19 actualizada.
Sin embargo, todos los ingredientes serían iguales en una nueva vacuna. La única diferencia serían unas pocas líneas de código genético que cambiarían ligeramente la forma de la proteína de pico.
Desde una perspectiva de seguridad, una vacuna actualizada es esencialmente idéntica a las vacunas ya probadas.
Debido a estas similitudes, es posible que las pruebas clínicas no necesiten ser tan extensas como las que se necesitaban para las vacunas COVID-19 de primera generación.
Como mínimo, los ensayos clínicos de vacunas actualizadas probablemente requieran pruebas de seguridad y la confirmación de que una vacuna actualizada induce niveles de anticuerpos a la par con la respuesta de la vacuna original contra las cepas original, beta y delta.
Si estos son los únicos requisitos, los investigadores inscribirían solo a cientos, no a decenas de miles, de personas para obtener los datos clínicos necesarios.
Una cosa importante a tener en cuenta es que si los fabricantes de vacunas deciden actualizar sus vacunas para la variante omicron, no sería la primera vez que realizan este tipo de cambio.
Una variante anterior, B.1.351, surgió en octubre de 2020 y era lo suficientemente resistente a las vacunas vigentes en ese momento como para justificar su actualización .
Los fabricantes respondieron rápidamente a la amenaza potencial desarrollando una vacuna de ARNm actualizada para coincidir con esta variante y realizaron ensayos clínicos para probar la nueva vacuna .
Afortunadamente, esta variante no se convirtió en la variante dominante. Pero si lo hubiera hecho, los fabricantes de vacunas habrían estado listos para lanzar una vacuna actualizada .
Si resulta que omicron, o cualquier variante futura, para el caso, justifica una nueva vacuna, las empresas ya completaron los ensayos generales y están listas para enfrentar el desafío.
Escrito por Deborah Fuller, profesora de microbiología, Facultad de Medicina, Universidad de Washington .